Aire cardiologie
Mieux comprendre et mieux soigner les maladies cardiovasculaires ou cardio-neurovasculaires avec MEDITWIN.
Vers une cardiologie plus précise
Le projet MEDITWIN comporte trois cas d'étude pilotes évaluant comment les jumeaux virtuels en cardiologie permettraient d’agir plus tôt et avec plus de précision dans les pathologies du système cardiovasculaire pour :
Accompagner les patients
Les maladies cardiovasculaires ou cardio-neurovasculaires constituent la première cause de mortalité et de perte d'années de vie en bonne santé dans le monde en 2021. Il s’agit d’un problème de santé mondial qui concerne 190 pays sur 204 étudiés, pour lequel ces maladies se situent parmi les cinq principales causes de perte d'années de vie en bonne santé [1].
La prévention et les progrès thérapeutiques de ces 40 dernières années ont permis une réduction de la mortalité globale mais de fortes disparités persistent, notamment dans les populations les plus à risques comme les personnes vivant avec un diabète ou une hypercholestérolémie familiale.
Outre la prévention, une prise en charge rapide des événements aigus et l’accès aux interventions cardiaques permettent de réduire les effets négatifs des maladies cardiovasculaires. Il est cependant essentiel de corriger les inégalités géographiques en matière d'accès et de qualité des soins [1].
Le projet MEDITWIN comporte trois cas d'étude pilotes évaluant comment les jumeaux virtuels en cardiologie permettraient d’agir plus tôt et avec plus de précision dans les pathologies du système cardiovasculaire pour :
- la prévention des risques cardiovasculaires chez les personnes vivant avec une hypercholestérolémie familiale
- la prévention des complications graves après infarctus
- la réalisation d’interventions cardiaques chez les nouveaux-nés
Prévenir les évènements cardiovasculaires chez les personnes avec hypercholestérolémie familiale
Les maladies cardiovasculaires représentent la première cause de mortalité dans le monde, et l'hypercholestérolémie est un facteur de risque solidement établi.
- 1 personne sur 300 est atteinte d’hypercholestérolémie familiale, une des plus fréquente maladie génétique.
- Environ 20 % des personnes présentant une coronaropathie ne sont pas traitées pour leur cholestérol.
- Environ 2,2 millions de Français (sur 45 millions d'adultes) ont été touchés en 2021 par la maladie athéromateuse cardiovasculaire (maladie qui se caractérise par une accumulation de plaques de cholestérol dans la paroi artérielle).
Pourquoi s'appuyer sur l'hypercholestérolémie familiale pour apprendre à réduire le risque cardiovasculaire à travers des jumeaux numériques ?
À ce jour, toute personne peut évaluer son risque cardiovasculaire avec l’aide de son médecin. En effet, certains facteurs mesurables comme le LDL-cholestérol sont incontestablement liés au risque de maladie cardiovasculaire. Néanmoins, ces marqueurs ne suffisent pas pour suivre finement la santé cardiovasculaire des personnes vivant avec une hypercholestérolémie familiale.
Sans outils de prédiction, il est difficile d’individualiser le suivi des patients et de choisir les traitements les plus appropriés, ainsi que les doses optimales, tout en réduisant les effets secondaires associés aux traitements (statines). Les équipes médicales ont choisi de prendre comme modèle les patients atteints d’hypercholestérolémie familiale car c’est une population ayant un risque beaucoup plus élevé de développer une maladie cardiovasculaire. L’idée est d’en modéliser les données médicales pour créer ensuite des jumeaux numériques.
Pr Bertrand Cariou, directeur de l’institut du thorax (CHU de Nantes)
Ce modèle d’hypercholestérolémie familiale sert, en quelque sorte, de démonstrateur. Le modèle de jumeaux numériques ainsi créé sera ensuite validé et généralisé dans d’autres populations à haut risque cardiovasculaire.
Comment le projet MEDITWIN peut-il aider à mieux évaluer et réduire le risque cardiovasculaire ?
MEDITWIN offrira la possibilité d’établir un modèle de jumeau virtuel combinant le système métabolique, le système cardiovasculaire et de la rétine pour suivre comment évolue la santé cardiovasculaire des personnes vivant avec une hypercholestérolémie familiale.
Les équipes de Dassault Systèmes et d'INRIA HEKA utiliseront notamment des approches statistiques avancées pour analyser les données cliniques, métabolomiques et génétiques. Cette approche permettra de mieux comprendre pourquoi certaines personnes développent une maladie cardiovasculaire ou sont victimes d’infarctus, ce qui permet d’anticiper et de réduire les risques chez les futurs patients, de mieux les prendre en charge et d’éviter les récidives.
Pourquoi combiner de multiples échelles dans les jumeaux virtuels ?
Les accidents cardiovasculaires sont majoritairement causés par une atteinte des artères dites "de gros calibre" comme les coronaires. Ces derniers seront d'autant plus graves si les petits vaisseaux sont également altérés (pouvant causer une altération de la résilience des organes à une agression). La rétine est le seul organe où l'on peut observer relativement facilement la circulation sanguine jusqu'aux plus petits vaisseaux sanguins, les capillaires. A titre d’exemple, une analyse par tomographie de cohérence optique permet de détecter des séquelles de "micro-infarctus" rétiniens, associés aux accidents cardiovasculaires.
Les jumeaux virtuels pourront participer à mieux comprendre le lien entre la micro et la macro-circulation dans un système cardiovasculaire sain pour ensuite mieux comprendre les mécanismes physiopathologiques dus au vieillissement, à l’hypertension, au diabète, etc. Par exemple, un jumeau de la circulation rétinienne permettra une analyse personnalisée de haute précision de l'état microcirculatoire, et autorisera également de suivre l'effet du traitement agissant sur la microcirculation, ce qui n'est pas possible actuellement. Avec les jumeaux numériques, la prise en charge deviendra individualisée.
Dr Matthieu Wargny (CHU de Nantes)
Ce projet MEDITWIN représente un réel espoir pour les patients souffrant de maladies cardiovasculaires.
Prévenir les arythmies ventriculaires graves après infarctus
Quel est le risque d'arythmies ventriculaires graves après un infarctus ?
Les arythmies ventriculaires graves peuvent survenir chez les personnes ayant subi un infarctus du myocarde dans un passé plus ou moins lointain. Il s’agit de perturbations du rythme cardiaque secondaires aux modifications des tissus après l'infarctus.
L'implantation d'un défibrillateur chez les patients ayant subi un infarctus peut permettre de réduire ce risque en détectant les épisodes de tachycardies ventriculaires et en régulant le rythme cardiaque. Néanmoins les critères de choix pour guider l'implantation d'un défibrillateur permettent d’identifier seulement 30% des personnes à risque.
Comment soigner les patients après un infarctus ?
Il est essentiel d’identifier précisément les personnes qui sont à risque de développer une arythmie ventriculaire grave après un infarctus. Le risque augmente proportionnellement à la taille de l’infarctus, ce que l’on détecte en mesurant la performance du muscle cardiaque à travers la fraction d'éjection qui va être abaissée (la fraction d'éjection correspond à la fraction de sang éjectée par le cœur dans le corps à chaque battement).
Malheureusement, c’est une évaluation rudimentaire et certains patients ont un risque de mort subite élevé malgré une fraction d’éjection modérément altérée. D'autres critères entrent en jeu et restent à identifier.
En quoi le projet MEDITWIN apporte-t-il un espoir dans la prévention des infarctus ?
Pour mieux identifier les patients à risque, les jumeaux virtuels s'appuieront sur les mesures faites par l’imagerie cardiaque (IRM) et par les électrocardiogrammes pour les combiner grâce aux connaissances des équipes médicales.
À partir de méthodes de recalage non-rigide et de segmentation 3D, ainsi que de modèles prédictifs probabilistes, les équipes de Dassault Systèmes, de l’IHU Liryc et d'INRIA EPIONE se pencheront sur le développement d'un jumeau numérique cardiaque permettant d’évaluer précisément le risque d'arythmies ventriculaires graves après infarctus et d’orienter ainsi efficacement les stratégies de prévention (par exemple l’implantation de défibrillateur).
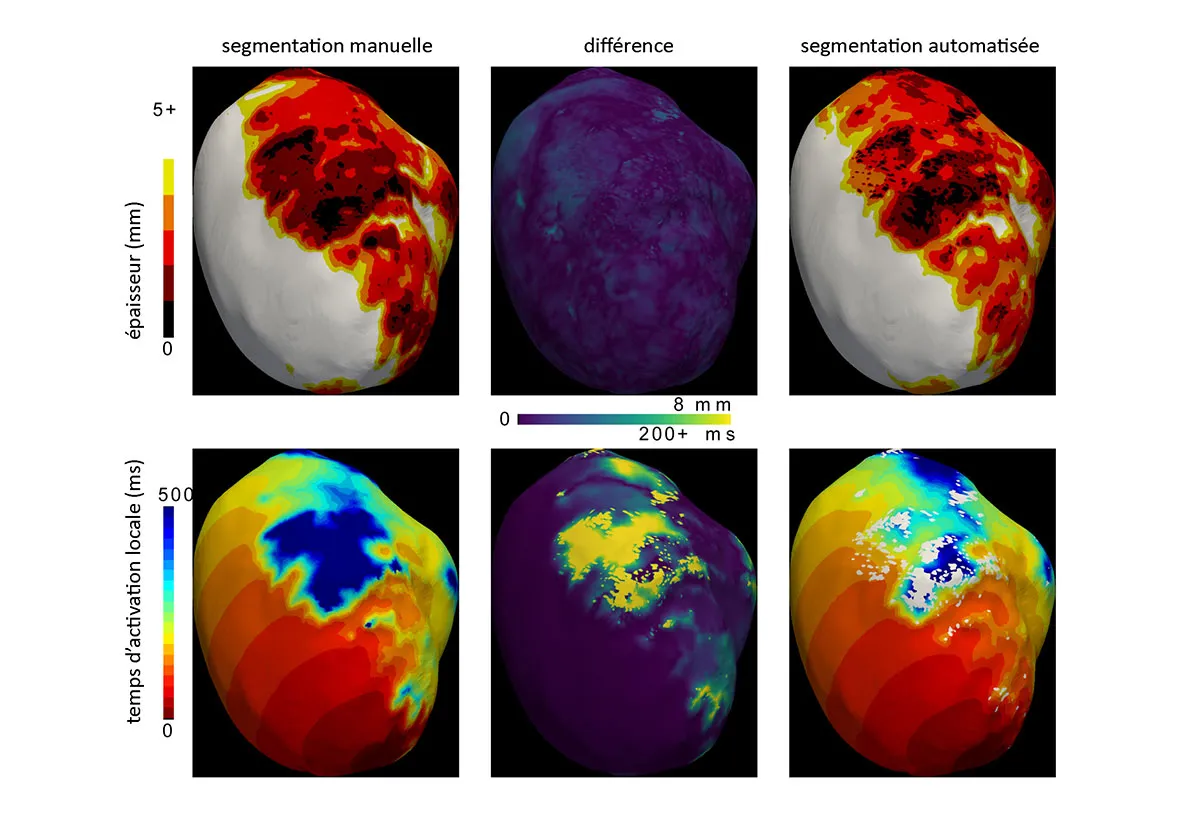
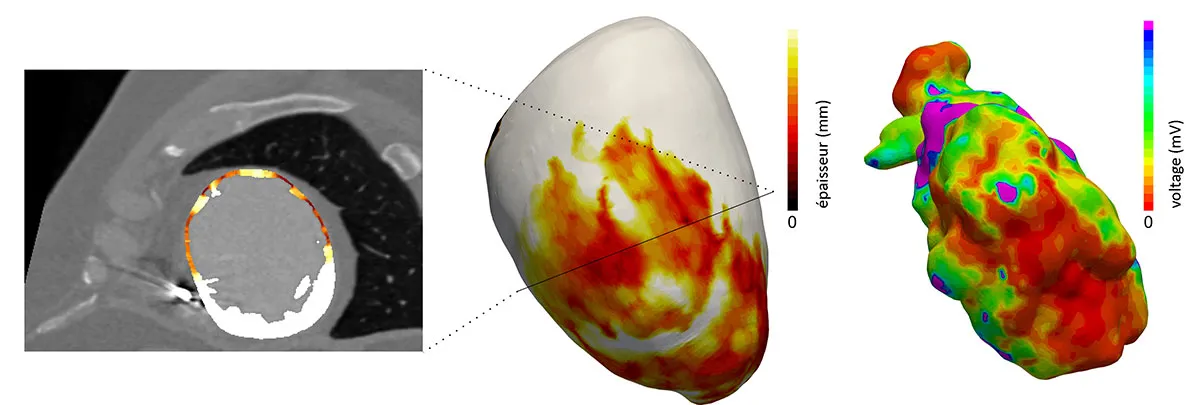
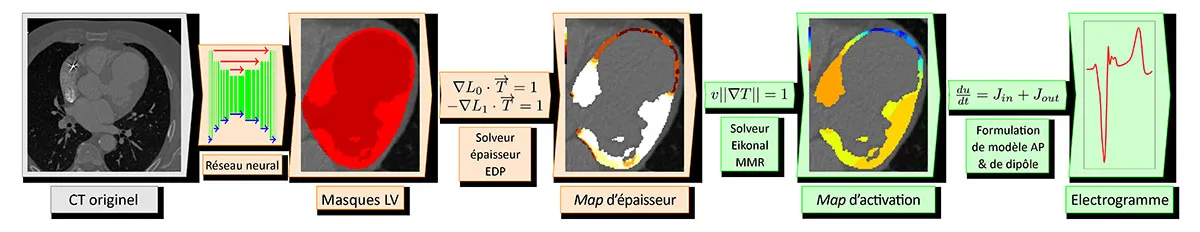
L’entreprise inHEART développe des technologies de segmentation 3D du cœur et des zones cicatricielles à partir d’images médicales issues du scanner et de l’IRM, afin de construire un jumeau numérique personnalisé du cœur.
Ce jumeau numérique sera progressivement enrichi par l’intégration de prédicteurs cliniques complémentaires, notamment dérivés de l’IRM et de l’ECG, afin de permettre une stratification précise du risque de mort subite chez les patients.
L’objectif global du projet est d’automatiser cette étape clé à l’aide de techniques d’intelligence artificielle, afin d’accélérer et de standardiser la préparation du jumeau numérique tout en garantissant un haut niveau de fiabilité et de reproductibilité des résultats.
Cardiopédiatrie : mieux prendre en charge l'hypoplasie du ventricule gauche chez le nouveau-né
Qu'est-ce que l'hypoplasie du ventricule gauche ?
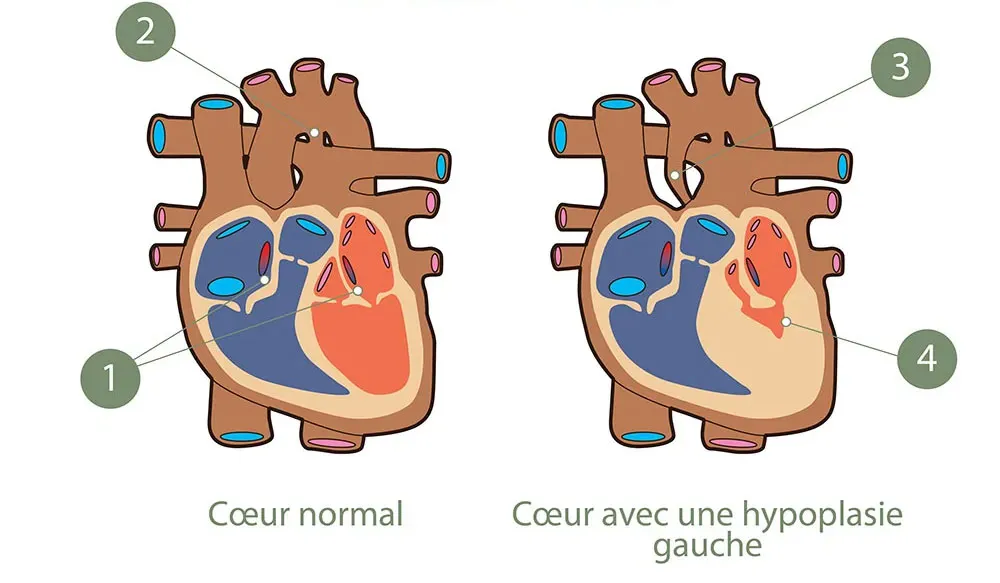
L'hypoplasie du ventricule gauche est une maladie rare caractérisée par une malformation congénitale cardiaque. Cette pathologie touche le ventricule gauche et les gros vaisseaux du cœur des nouveau-nés. Elle est caractérisée par un développement insuffisant du ventricule gauche qui n’exerce plus son rôle de pompe.
Ces nouveau-nés doivent subir plusieurs interventions cardiaques dans les premières semaines et les premières années de vie pour rétablir une circulation sanguine efficace dans le corps entier avec un seul ventricule.
Quels sont les défis pour soigner les nouveau-nés vivant avec cette pathologie ?
L'hypoplasie du cœur gauche est la cardiopathie la plus sévère, impactant la survie et la qualité de vie pour les nouveau-nés. Elle nécessite une intervention chirurgicale rapide dès les premiers jours après la naissance. Plusieurs intervention complexes pouvant coupler intervention chirurgicale et cathétérisme dans les artères pulmonaires seront nécessaires.
Les nouveau-nés ayant subi une intervention chirurgicale doivent faire l'objet d'un suivi médical important pour prévenir les complications et permettre une meilleure qualité de vie. Celle-ci doit être coordonnée sur le long terme et adaptée à chaque patient. Aujourd’hui, les médecins doivent souvent prendre des décisions critiques avec des informations limitées sur l'évolution de la maladie et l'efficacité des traitements.
Qu’apporte le projet MEDITWIN à la cardiopédiatrie ?
Avec le développement de jumeaux virtuels du cœur personnalisés des nouveau-nés, les chirurgiens et les médecins pourront :
- identifier les zones anatomiques du système cardio-vasculaire à corriger
- apprécier l’impact des différentes interventions possibles sur les mesures physiologiques
- prendre en compte l'évolution de l'état du patient avant et pendant l'opération pour assurer un suivi du patient tout au long de sa croissance
Deux équipes-projets Inria sont impliquées dans ce projet :
- L’équipe-projet COMMEDIA développera des modèles numériques d’écoulement sanguin basés sur des équations de la mécanique des fluides (équations de Navier-Stokes). Ces simulations par méthode des éléments finis permettront de représenter précisément la dynamique cardiaque chez les nouveau-nés souffrant d'hypoplasie du ventricule gauche. Ces modèles virtuels fourniront un outil essentiel pour la planification préopératoire, optimisant ainsi la prise en charge chirurgicale et le suivi médical personnalisé des jeunes patients.
- L’équipe-projet SIMBIOTX développera des modèles multi-échelles couplant des approches dites « zéro-D » (modèles compartimentaux à paramètres concentrés), « un-D » (flux dans les réseaux vasculaires), et « trois-D » (simulation hémodynamique détaillée par éléments finis). L’intégration de ces modèles au sein d'un jumeau numérique spatio-temporel permettra de simuler l’évolution biologique et physiologique des enfants atteints de pathologies cardiaques complexes, comme le syndrome du cœur gauche hypoplasique, facilitant ainsi la prise de décisions cliniques critiques.
Reférences
Global incidence, prevalence, years lived with disability (YLDs), disability-adjusted life-years (DALYs), and healthy life expectancy (HALE) for 371 diseases and injuries in 204 countries and territories and 811 subnational locations, 1990–2021: a systematic analysis for the Global Burden of Disease Study 2021 Ferrari, Alize J et al. The Lancet, Volume 403, Issue 10440, 2133 - 2161