Quand les données sauvent des vies
L’utilisation de données d’origines, de sources et de formats divers, parfois hétérogènes constitue un axe de progrès pour la recherche médicale.
L’utilisation de données d’origines, de sources et de formats divers, parfois hétérogènes (et qui ne sont généralement pas rassemblées et combinées) constitue un axe de progrès particulièrement fécond pour la recherche médicale. Restructurées et mises en relation, ces données s’enrichissent mutuellement et constituent un actif porteur de promesse de progrès thérapeutique.
Pour étudier la Covid-19, les chercheurs ont par exemple utilisé des bases de données rassemblant les demandes de remboursement auprès des assurances, des données démographiques ou liées au mode de vie, produites par des organismes de crédit ou par l’administration gouvernementale. Ces données, aux côtés de celles issues de laboratoires, viennent en appui des études, achevées ou en cours, sur l’impact de la Covid-19 auprès de populations spécifiques ou portant sur des prédictions d’hospitalisation.
Cependant, lorsqu’on évoque l’utilisation généralisée de données recoupées, restructurées et agrégées, se pose immédiatement la question de leur confidentialité. En effet, la data n’est pas constituée de chiffres abstraits, elle est intimement liée à l’expérience du patient, du citoyen. L’utilisation de ses données personnelles doit être précisément encadrée, mais des règles trop strictes empêcheraient justement d’utiliser efficacement ces données, notamment si elles interdisaient l’individualisation, la corrélation et l’inférence.
L’individualisation, ou singularisation, signifie qu’au sein d’un groupe, il est possible de déterminer qui est une personne à laquelle les données se rapportent. La corrélation signifie qu’il est possible de connecter des données provenant de différentes sources à une personne unique. Et l’inférence signifie qu’il est possible de déduire quelque chose sur une personne simplement parce qu’elle fait partie d’un groupe. Ainsi, même s’il n’est pas possible de donner un nom à la personne en question, si l’un de ces trois éléments est possible, l’ensemble de données ne pourra pas être considéré comme anonyme.
Maintien du secret médical et confidentialité
En outre, les entreprises pharmaceutiques et informatiques travaillent sur des solutions pour mener à distance ou à domicile des études. Le recueil du consentement du patient soulève alors de nouvelles questions d’identification, de maintien du secret médical et de confidentialité. Les services à distance doivent en effet être mis en œuvre avec la même confidentialité que lors d'un face à face dans le cabinet du médecin, derrière une porte close. La ségrégation complète des données, séparées physiquement et logiquement, constitue sans doute une partie de la solution.
Or, un grand laboratoire pharmaceutique, lorsque les essais cliniques sont lancés, transfère des données personnelles dans le monde entier, notamment pour des raisons de soumission de celles-ci aux régulateurs, et de respect de la législation. Après autorisation de mise sur le marché, la pharmacovigilance nécessite également d’évaluer des données issues de différents pays.Les données transitent donc d’un pays à l’autre. Il est alors indispensable de disposer de moyens légaux pour transférer, par exemple, des données de l’Union européenne vers les États-Unis.
Favoriser le consentement éclairé du patient
Lorsqu’un patient intègre un essai clinique, il passe par plusieurs étapes, qui commencentpar son implication dans le processus de consentement éclairé. Or, 35 % des patients potentiels refusent d’entrer dans un essai clinique parce qu’ils disent ne pas comprendre les informations qui leur sont données. Les patients utilisant le consentement sur papier montrent un taux de compréhension plus faible que ceux l’utilisant sous forme électronique, qui permet une pédagogie faisant appel à différents modes de communication.
Avec eConsent, la solution de consentement électronique et à distance développée par MEDIDATA, les patients passent plus de temps à se renseigner sur l’essai clinique, et comprennent mieux l’objectif, les avantages, les risques d’une étude ainsi que leurs droits et responsabilités. eConsent améliore donc l’éducation et l’engagement des patients, ce qui se traduit également par une amélioration de la conformité et de la fidélisation au sein de l’étude.
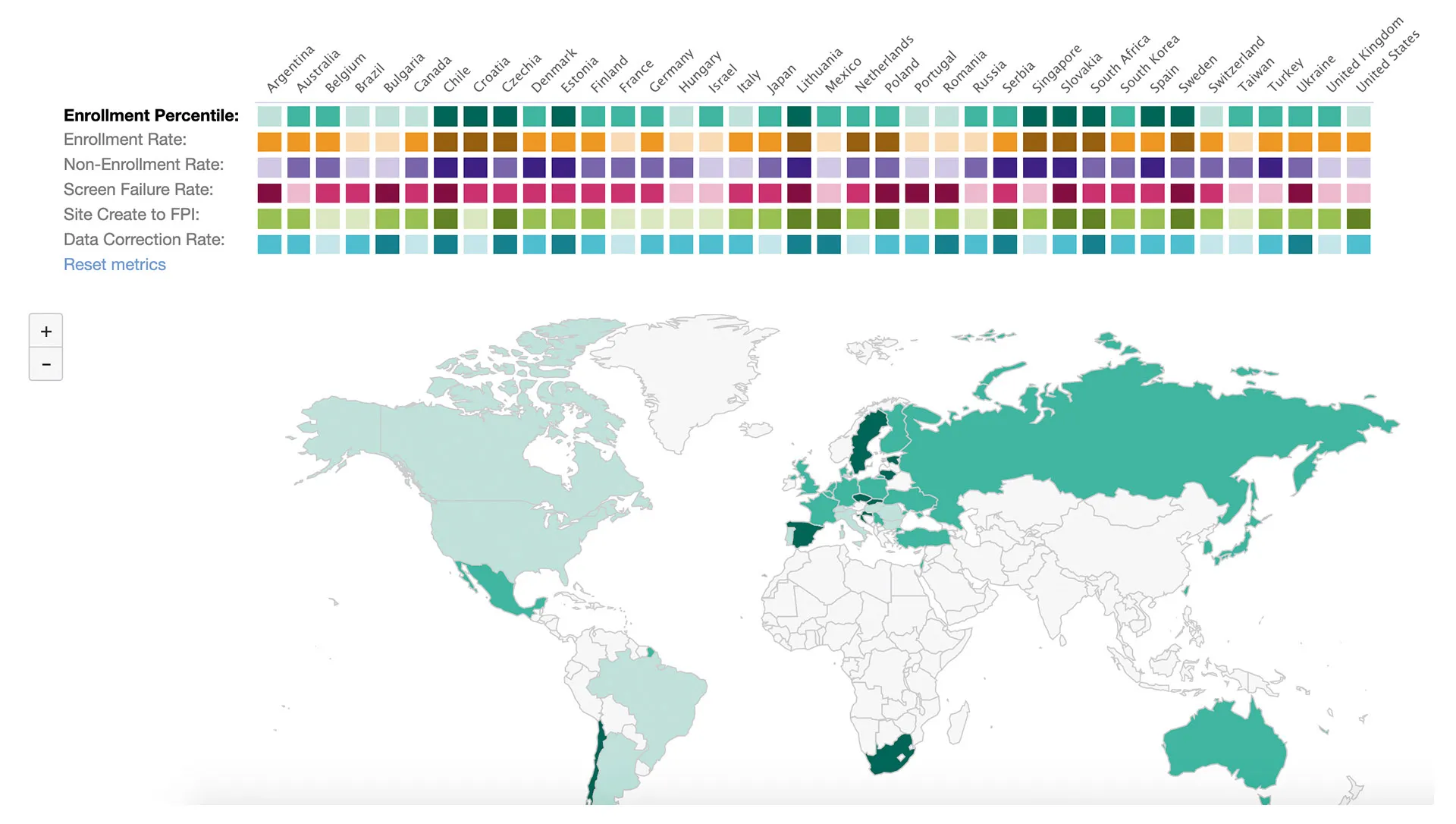
Traiter et exploiter les données
Acorn AI, filiale de Medidata, utilise des données cliniques uniques, des analytiques avancés et une expertise humaine développées depuis vingt ans pour supporter la croissance des entreprises des sciences de la vie en accélérant leur développement sur le marché. La solution Intelligent Trial fournit notamment des données d’essais cliniques opérationnels intersectoriels en temps réel, permettant aux clients d’acquérir un avantage concurrentiel en exécutant des essais cliniques avec une agilité accrue.
Après l’acquisition et le traitement, l’exploitation nécessite aussi une expertise particulière des données. MEDIDATA Detect est un outil d’analyse statistique centralisé dont les algorithmes aident les chercheurs à interroger les données cliniques en mettant l’accent sur leur qualité et la sécurité des patients. La solution permet notamment, à partir d’expériences utilisateur différentes et complexes, de sources disparates et hétérogènes, de standardiser, d‘agréger, de rassembler les données.
MEDIDATA a simplifié ces analyses avancées en adoptant une approche de plateforme, les données circulant automatiquement sur le cloud,sans qu’il soit nécessaire de réaliser une extraction ou de télécharger les données.
Synthetic Control Arm®, la solution de bras de contrôle externe de MEDIDATA, utilise des données d’essais cliniques historiques et intersectorielles au niveau des patients pour remplacer ou compléter les bras de contrôle, en particulier dans les maladies dépourvues d’équilibre clinique. Ainsi, le bras de contrôle synthétique peut accélérer le développement clinique dans des situations dans lesquelles les essais contrôlés randomisés traditionnels ne sont pas réalisables ou imposent une charge indue aux patients.
Le comité européen de la protection des données a énoncé les bases juridiques sur lesquelles s’appuyer dans le cadre d’un essai clinique.