Médecine translationnelle, thérapies ciblées et sciences omiques
Grâce à une approche en réseau collaboratif, la médecine translationnelle et les thérapies ciblées peuvent accélérer la recherche sur les maladies rares.
Le Dr David Fajgenbaum a changé la manière dont la maladie de Castleman est comprise et traitée. Il avait été diagnostiqué avec une forme de la maladie orpheline (maladie de Castleman multicentrique idiopathique) et est maintenant en rémission en raison d’un traitement de précision qu’il a identifié lui-même. Il a en effet créé et dirige une fondation, le Castleman Disease Collaborative Network, pour accélérer la recherche et les traitements de la maladie grâce à une approche en réseau collaboratif, faisant à la fois appel à la médecine translationnelle et aux thérapies ciblées, une approche devenue un modèle pour d’autres maladies rares.
Elle intègre les vues des patients pour guider une recherche à fort impact et identifier les traitements qui peuvent être réutilisés contre la maladie de Castleman. Les sciences omiques, telles que la génomique, la protéomique, la transcriptomique et la métabolomique, ont permis le développement de nouvelles technologies : biocapteurs, outils diagnostiques, traitements. Le Dr Fajgenbaum l’affirme : “L’intégration des données cliniques sur la plateforme MEDIDATA Omics a vraiment transformé notre analyse et notre interprétation des données protéomiques.” En lui sauvant la vie, et celle de milliers d’autres patients.

En octobre 2020, Medidata a finalisé l’acquisition de MC10, société spécialisée dans le développement de biomarqueurs, permettant de contrôler l’état du patient ou sa réponse à un traitement. Déjà utilisées dans de nombreux essais cliniques, les offres de MC10 apportent de nouvelles capacités d’analyse aux solutions Patient Cloud de MEDIDATA, notamment pour enrichir les données apportées par les patients (ePRO), ou pour l’évaluation des résultats d’essais cliniques (eCOA).
Les acteurs de la santé disposeront ainsi d’encore plus de moyens pour gérer virtuellement les essais cliniques. Car les données, issues du monde réel, révèlent toute leur puissance lorsqu’elles peuvent rétroagir sur celui-ci, notamment à travers des dispositifs médicaux.
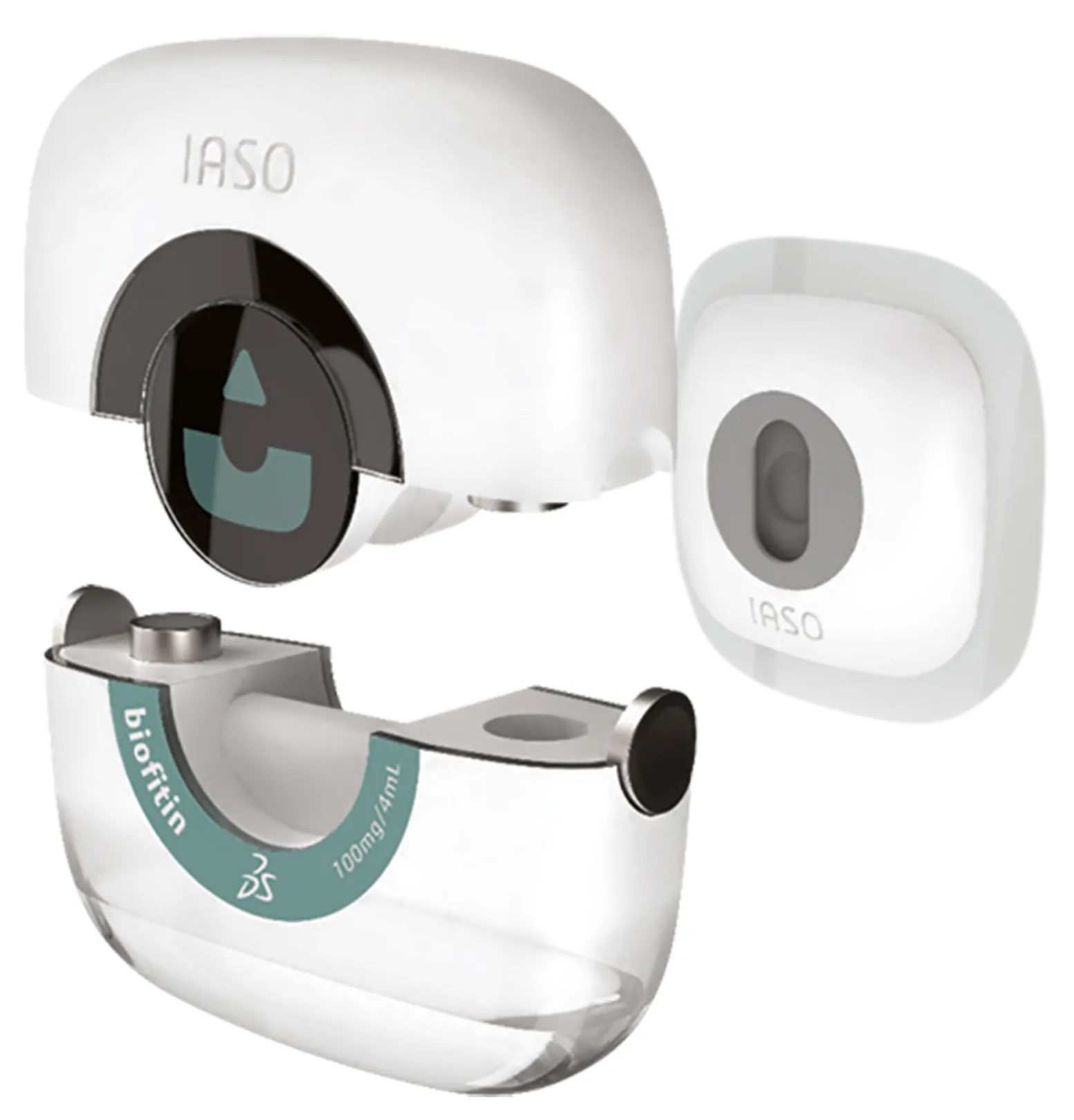
Dans le cadre de la recherche sur les dispositifs, IASO, inspiré du nom de la déesse grecque de la guérison, est ainsi un démonstrateur illustrant le cycle de vie d’un produit biologique combiné à un auto-injecteur, destinés à l’oncologie. Il démontre la valeur que la plateforme 3DEXPERIENCE peut apporter aux acteurs cherchant à innover dans le domaine des médicaments combinés à un dispositif médical.
Accélérer l’innovation avec l’expérimentation in silico
IASO illustre la façon dont la conception 3D, l’ingénierie collaborative et la simulation numérique font progresser le développement de médicaments candidats et de dispositifs médicaux. À l’étape de fabrication, il montre comment les entreprises peuvent organiser l’usine du futur, en imaginant de nouvelles solutions de planification et d’exécution.
Enfin, IASO démontre comment la plateforme 3DEXPERIENCE favorise l’excellence opérationnelle, en optimisant les activités réglementaires et le système de gestion de la qualité, et en fournissant une vue transversale et unifiée de l’expérience patient.S’appuyer uniquement sur l’expérimentation physique n’est en effet pas viable économiquement, notamment dans l’environnement Covid-19 en évolution rapide.
Les scientifiques ont besoin de mieux comprendre comment les thérapies antivirales et les vaccins fonctionnent. Pour aider les chercheurs à identifier des molécules avec de nouvelles propriétés, BIOVIA a développé BIOVIA Discovery Studio, un environnement de modélisation et de simulation qui fournit aux chercheurs un ensemble complet d’outils, notamment des moyens de conception et d’analyse de produits biologiques, des simulations classiques, une conception basée sur la structure des fragments et le criblage virtuel, visant à identifier des molécules aux propriétés nouvelles.
La solution intègre également la simulation pharmacocinétique du signal ADME (absorption, distribution, métabolisme et excrétion) et la prédiction de la toxicité de la molécule étudiée
Le modèle a été construit avec BIOVIA Discovery Studio en utilisant la structure PDB 6M17 (récepteur ACE2 humain en complexe avec domaine RDB de la protéine spiculaire SARS-CoV-2) et 7DK4 (protéine spiculaire SARS-CoV-2 en conformation stabilisée pré-fusion avec deux domaines RBD vers le haut) en superposant les deux structures sur le domaine RDB commun.